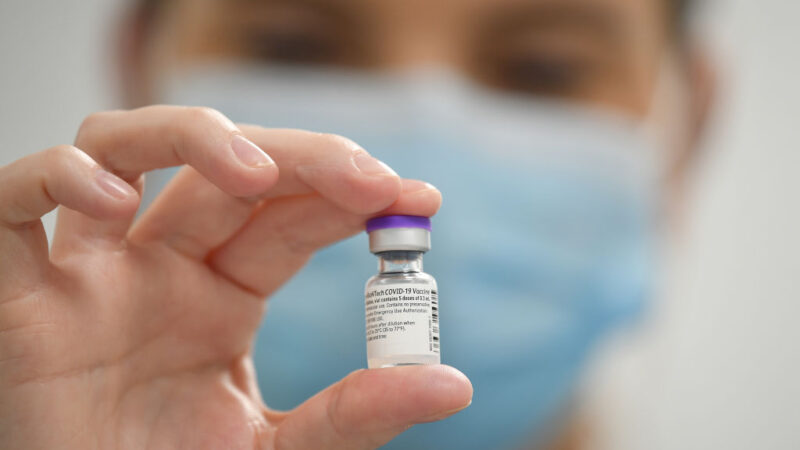
【新唐人北京時間2021年09月18日訊】美國食品藥品管理局(FDA)的諮詢委員會9月17日建議,不要為16歲及以上的人群追加第三劑輝瑞疫苗。
在整個會議期間,FDA的獨立科學家們對是否有必要為普通民眾接種第三劑輝瑞公司的mRNA 中共病毒(COVID-19)疫苗,以增加免疫功能持懷疑態度。最後,科學家們以16:3的投票結果建議不對16歲以上人群加強注射。(點擊觀看相關視頻)
為強化反對向普通人群推薦加強劑的論點,專家提供的一份幻燈片顯示,一個30歲健康的人其染疫風險只有0.0004%或1/25萬。而對年齡較大的人打第三針疫苗可能將增加罹患心肌炎的風險。
FDA在決定藥物核准和相關規定前,往往會參考諮詢委員會的意見。目前,FDA和CDC僅允許準備讓器官移植者,或免疫系統較脆弱的人追加接種第三劑疫苖。
不過,17日的初步結果或讓聯邦的疫苗接種議程面臨一次重大的考驗。衛生與公眾服務部(HHS)已在15日宣布,從9月20日開始大規模向民眾提供第三劑疫苗。這項措施因爲忽略FDA正在權衡輝瑞的申請和免疫實踐諮詢委員會的考量,而備受爭議。
據NPR報導,現階段被提出來支持施打第三劑疫苗的因素包括,一些數據表明,輝瑞疫苗的防護力會隨著時間拉長減弱,以及具有高傳播性的Delta病毒株造成多個國家的確診率激增。
但17日會議的報告普遍顯示,在美國,該疫苗在保護人免受嚴重疾病、住院和死亡方面仍然有效。
在會議期間,來自FDA、輝瑞公司、CDC、以色列和英國方面的發言人分別介紹了有關該大流行病的數據、接種輝瑞疫苗的經驗和實驗室測試。
(記者陳北晨綜合報導/責任編輯:林清)
本文網址: https://www.ntdtv.com/b5/2021/09/17/a103219142.html